Segovia recibirá un primer envío con 1.950 vacunas
El miércoles 30 de diciembre está previsto que se inicie la administración de las vacunas. Hasta el 15 de marzo del 2021 nuestra provincia recibirá 20.475 dosis
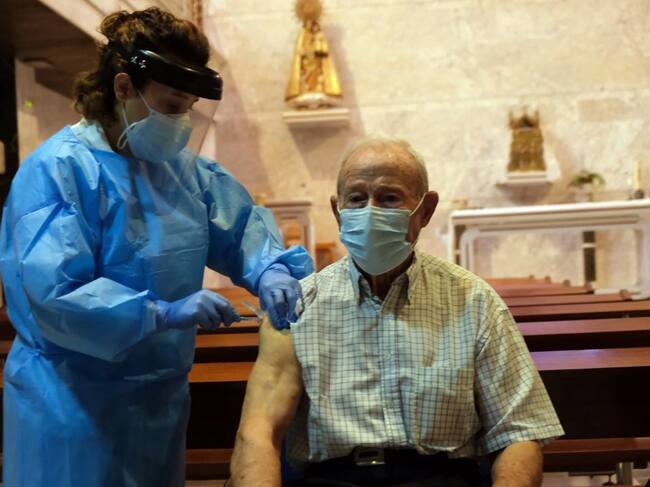
Áureo López García recibe la primera dosis de la vacuna. / JCYL (EUROPA PRESS)

Segovia
La residencia de ancianos de la localidad palentina de Cevico de la Torre ha sido el lugar elegido por la Junta de Castilla y León para iniciar hoy, en coincidencia con el resto de comunidades españolas y países de la Unión Europea, el primer ciclo de la estrategia de vacunación frente a la COVID-19 establecida por el Ministerio de Sanidad y la Consejería de Sanidad.
En total se han vacunado 82 residentes (la totalidad del centro) y 40 trabajadores. El primer residente vacunado ha sido Áureo López García, de 88 años, y la primera trabajadora, Domitila Bilbao Calleja.
Segovia recibirá un primer envío con 1.950 vacunas para comenzar a administrarlas el miércoles 30 de diciembre. Hasta el 15 de marzo del 2021 nuestra provincia recibirá 20.475 dosis.
La previsión comunicada a la Administración autonómica por el Gobierno central es que, a partir de mañana, día 28, irán llegando a las nueve provincias de la Comunidad, con periodicidad semanal y hasta el 15 de marzo, el total de 322.440 dosis anunciadas para completar los dos primeros de los tres ciclos previstos en esta fase de la estrategia de vacunación.
Esta primera etapa contempla cuatros grupos priorizados de población diana: los residentes y personal sanitario y sociosanitario en residencias de personas mayores y con discapacidad; el personal sanitario de primera línea; otro personal sanitario y sociosanitario; y grandes dependientes no institucionalizados.
Vacuna
La vacuna que se va a distribuir en esta primera fase es la desarrollada por los laboratorios de Pfizer/BioNTech. Como se sabe, requiere dos dosis para completar su efectividad, existiendo un plazo entre la primera y la segunda dosis de veintiún días; es necesario, por ello, una compleja organización, planificación y logística para poder aprovechar el máximo de unidades con la mínima pérdida en la cadena de frío o el transporte de dosis.
Se trata de un medicamento que ha obtenido la aprobación de la Agencia Europea del Medicamento (EMA) tras haber superado los análisis de calidad y seguridad, habiendo sido testada en más de 44.000 voluntarios de dieciséis o más años en su fase III, siendo las reacciones adversas observadas más frecuentemente la fatiga (62,9 %), cefalea (55,1 %), dolores musculares (38,3 %), escalofríos (31,9 %) y fiebre (14,2 %), efectos similares a los de la vacuna de la gripe y que remiten con medidas sencillas o medicación habitual.





