Sanidad aprueba la financiación de un fármaco que ralentiza la progresión de la ELA
España será uno de los primeros países de Europa en incorporar el medicamento al sistema público de salud

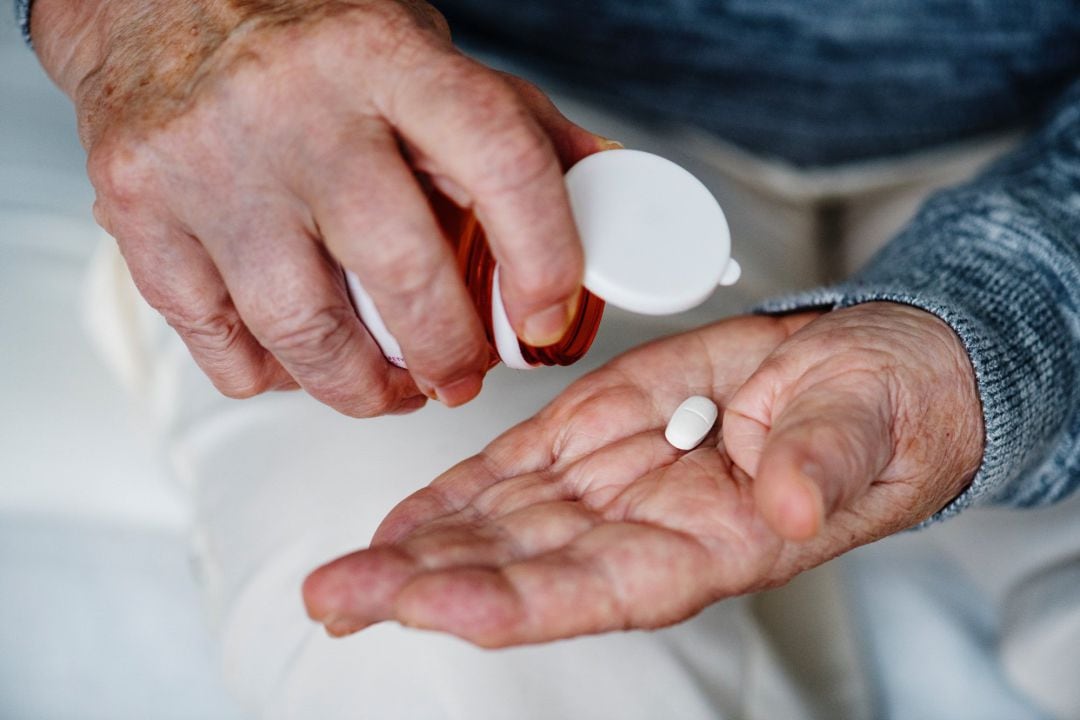
Medicamentos cáncer, fármacos, cáncer, adherencia al tratamiento / CEDIDA / FUNDACIÓN ECO - Archivo (EUROPA PRESS)
Madrid
El Ministerio de Sanidad ha aprobado este jueves la financiación de un medicamento que ralentiza la progresión de la esclerosis lateral amiotrófica, comúnmente conocida como ELA. El fármaco, llamado tofersén, se trata de una terapia innovadora que, además, preserva la función neuronal de la persona que padece la enfermedad.
Más información
España se convertirá, de esta forma, en uno de los pocos países europeos en incorporar este medicamento al sistema público de salud y que se trata del primero aprobado por la Unión Europea que actúa directamente sobre una causa genética conocida de la ELA.
La decisión tomada por la Comisión Interministerial de Precios de los Medicamentos (CIPM) de incluirlo en la prestación farmacéutica del Sistema Nacional de Salud supone una innovación en un área terapéutica donde no se producían incorporaciones farmacológicas desde los años 90.
El uso del fármaco requiere la identificación de la proteína SOD1 mutada a través de una prueba que se encuentra disponible en gran parte de los centros de referencia de ELA, presentes en la mayoría de las comunidades.
En sus redes sociales, la ministra de Sanidad, Mónica García, ha celebrado la incorporación de este tratamiento a la prestación farmacéutica. "Viva la sanidad pública", ha aplaudido.
El origen de tofersén
Tofersén fue autorizado por la Agencia Europea de Medicamentos (EMA) en mayo de 2024 bajo “circunstancias excepcionales”, dado que se trata de una enfermedad rara y los datos clínicos disponibles son limitados; cuenta además con la designación de medicamento huérfano, lo que reconoce su valor terapéutico en condiciones de alta necesidad médica no cubierta.
Descubre la nueva app de Cadena SER Te ofrecemos una mejor experiencia de audio y video
DescargarEl pasado lunes, la Agencia Española del Medicamento y Productos Sanitarios (Aemps) publicó el informe de posicionamiento terapéutico para este medicamento en el que se considera tofersen como una opción terapéutica para el tratamiento de adultos con ELA, asociada a una mutación en el gen de la proteína superóxido dismutasa 1 (SOD1) que ha demostrado efecto en biomarcadores relacionados con su mecanismo de acción.
La confirmación formal de beneficio clínico requerirá de los datos adicionales de eficacia y seguridad maduros y de la revaluación anual de la evidencia que se vaya generando.





