El CNIO crea el "reparoma humano", un catálogo de cicatrices del ADN que abre la puerta a terapias personalizadas contra el cáncer
La base de datos abierta REPAIRome, creada en España, permitirá a los investigadores de todo el mundo comprobar rápidamente cómo cada uno de los 20.000 genes humanos afecta a la reparación del ADN

De izquierda a derecha: los investigadores del CNIO Israel Salguero, Daniel Giménez, Ernesto López y Felipe Cortés. Crédito Marina Bejarano / CNIO

Lo que nos ha pasado en nuestra vida se puede medir, de alguna manera, por nuestras cicatrices. Y esas heridas permanentes, cerradas durante la curación de lo que nos ha pasado, también están en nuestro ADN. Ocurre cuando nos exponemos mucho al sol, o a productos carcinógenos. Las células intentan reparar las roturas en la cadena y, al reparar, dejan "marcas" que los científicos identifican como cicatrices.
Un equipo del Centro Nacional de Investigaciones Oncológicas, encabezados por Felípe Cortés, Ernesto López de Alba, Israel Salguero Corbacho y Daniel Giménez Llorente, ha creado un concepto pionero en biomedicina: el reparoma humano o REPAIRome, un catálogo que recoge cómo cada uno de los aproximadamente 20.000 genes humanos influye en la reparación del ADN. El trabajo se publica hoy en la revista Science. En declaraciones a la SER, Cortés asegura que "si podemos entender esas marcas que quedan en el ADN estaremos más cerca de tratamientos personalizados, terapias distintas para cada paciente".
El proyecto identifica y clasifica las "cicatrices" que se quedan en las cadenas de ADN tras sufrir una rotura y auto-repararse. Han generado un mapa de patrones mutacionales de enorme valor para la investigación del cáncer y los propios médicos que se enfrentan a la enfermedad en primera línea.

Infografía sobre el reparoma humano Crédito CireniaSketches
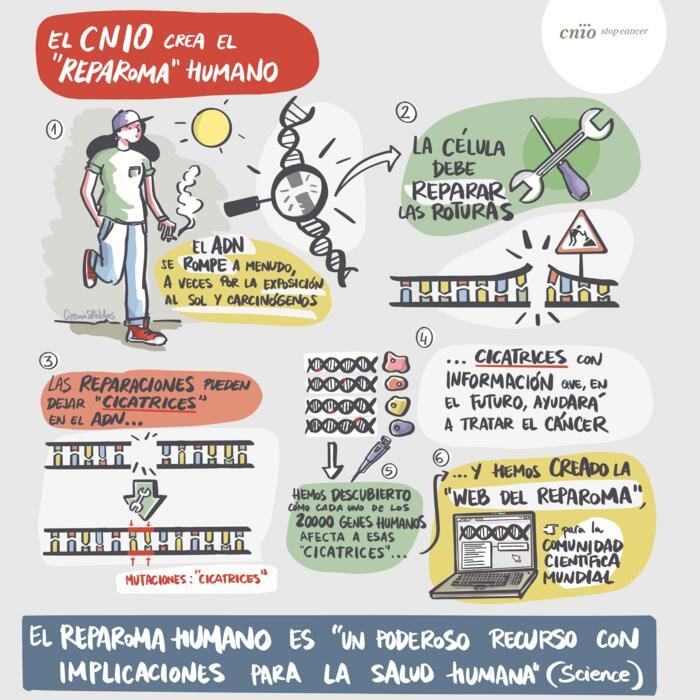
Infografía sobre el reparoma humano Crédito CireniaSketches
"Es un recurso poderoso para la comunidad científica, con implicaciones directas en la salud humana y en el tratamiento del cáncer", señalan los autores en Science. Y además en abierto.
Un recurso para todo el mundo científico
El portal web REPAIRome ya está disponible para investigadores de todo el mundo. Si entramos, vemos "mapas" de cómo afecta la pérdida o presencia de cada gen a la reparación del ADN.
Según Cortés, que es jefe del grupo de Topología de ADN y Roturas de ADN del CNIO y autor principal, el catálogo es "una plataforma para nuevos descubrimientos" que permitirá interpretar mejor las huellas moleculares en tumores y orientar tratamientos personalizados.
El equipo ha demostrado que decodificar estas cicatrices puede ayudar a predecir la respuesta de los tumores a terapias basadas en dañar el ADN, como la radioterapia o ciertos fármacos. El reparoma permitirá también trabajar en un campo, el de las herramientas de edición genética CRISPR-Cas, que dependen precisamente de inducir roturas en la doble hélice de nuestro ADN y que ya está dando resultados.
Cómo se hizo
Para elaborar el catálogo, los investigadores del CNIO "apagaron" uno a uno los 20.000 genes humanos en poblaciones celulares, provocaron roturas en la cadena con herramientas CRISPR y analizaron las cicatrices resultantes. Después del "bombardeo", el análisis computacional de todos esos datos permitió generar el mapa completo de huellas mutacionales.
“Ha sido un esfuerzo extenuante y minucioso porque hay unos 20.000 patrones, tantos como genes hay en el ADN humano”, señala Ernesto López, coautor del trabajo.
Ya está dando resultados
El estudio ya ha dado lugar a hallazgos concretos: entre ellos, un patrón de mutaciones asociado al cáncer de riñón y a condiciones de hipoxia (falta de oxígeno) en el paciente.
También se han identificado nuevas proteínas que intervienen en la reparación del ADN, tanto potenciando como bloqueando el proceso. Son solo los dos primeros logros y abre la puerta a vías terapéuticas innovadoras.
Reacciones
En declaraciones a Science media center, Andrés Aguilera, catedrático de Genética en la Universidad de Sevilla y jefe del grupo Inestabilidad Genómica y Cáncer en el Centro Andaluz de Biología Molecular y Medicina Regenerativa (CABIMER), dice:
“Los autores han analizado el efecto que causa la desactivación de más de 18.000 genes humanos, uno a uno, en la reparación de las roturas cromosómicas. Desactivaron cada gen mediante la técnica de CRISPR y determinaron el patrón de deleciones e inserciones que se acumulan como consecuencia de dicha reparación. Mediante un elaborado análisis computacional han sido capaces de establecer patrones comunes entre diferentes genes desactivados.
La constatación de que la desactivación de genes conocidos de reparación presenta los mismos patrones, así como un análisis profundo de algunas mutaciones específicas, validan el estudio realizado. No solo han logrado definir la huella dejada por las roturas cuando no funcionan genes y procesos específicos de reparación, sino que han descubierto nuevas funciones e interacciones genéticas de las proteínas de reparación, que deberán analizarse en profundidad en el futuro. Se ha generado una base de datos de enorme utilidad para el estudio de la reparación del ADN y su asociación de patrones específicos de mutaciones que se pueden encontrar en diferentes tumores.
El trabajo es muy novedoso, al establecer conexiones funcionales entre diferentes genes y procesos de reparación a través de la huella que su desactivación deja en el genoma, medida como deleciones e inserciones de nucleótidos.
El trabajo es de una excelente calidad, validado por la identificación de redes ya conocidas de interacciones funcionales entre genes, además de otras nuevas. Puede servir para asignar grupos de tumores a mutaciones en genes de reparación específicos según el patrón de deleciones o inserciones que acumulen dichos tumores, además de establecer nuevas relaciones funcionales entre procesos celulares diferentes.

Javier Ruiz Martínez
Redactor de temas de sociedad, ciencia e innovación en la SER. Trabajo en el mejor trabajo del mundo:...





