El remdesivir, único medicamento autorizado para el COVID-19 en EEUU
La farmacéutica Gilead sube un 7% en bolsa tras ser la primera en recibir la autorización para fabricarlo como tratamiento para tratar a los pacientes mas graves de la enfermedad, pero la OMS no lo respalda

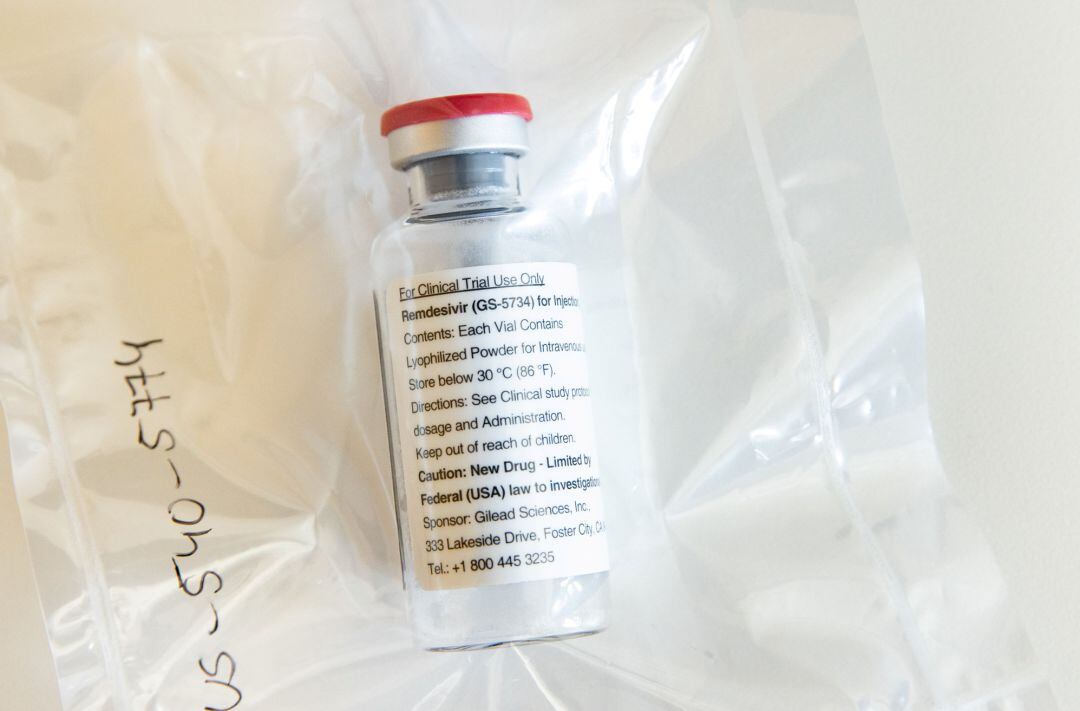
Un frasco con el antiviral remdesivir, de Gilead Sciences. / POOL (Reuters)
Madrid
La polémica está servida. Estados Unidos respalda el uso de remdesivir para tratar a pacientes graves hospitalizados por COVID-19 y la OMS dice todo lo contrario: que tras analizar este y otros medicamentos con centenares de pacientes en 30 hospitales de todo el mundo no se ha demostrado su eficacia, ni siquiera en reducción de la mortalidad.
Más información
Antes de que se publicara el informe de la OMS, echando por tierra con datos empíricos la efectividad del remdesivir, la Unión Europea había firmado un contrato para comprar miles de dosis por valor de mil millones de euros para suministrar a los 27 estados miembros el tratamiento. Teniendo en cuenta que un ciclo con tratamiento intravenoso de remdesivir cuesta alrededor de 2.000 euros y que, dos días después de la firma de compra, la OMS publica que no es eficaz, la regulación ahora por parte de la autoridad norteamericana vuelve a situarnos en una meseta de desconocimiento.
Según estudios realizados por centros nacionales de salud de EEUU con pacientes graves a los que se les suministró remdesivir, se ha conseguido reducir su tiempo de recuperación en 10 días, además de aliviar su sintomatología. En base a esos estudios, la autoridad reguladora de medicamentos y alimentos de EEUU (FDA) ha aprobado a la farmacéutica Gilead, con sede en California, su uso generalizado para pacientes que requieran hospitalización y estén graves. Y tras anunciar la noticia, las acciones de la farmacéutica se dispararon en bolsa un 7%. Gilead llevaba usando Remdesivir, como tratamiento experimental durante la pandemia, y ahora la FDA concede la aprobación final para casos de enfermos COVID-19 hospitalizados y graves.
El CEO de la farmacéutica, Daniel O'Day, explicaba que el remdesivir, no es una cura para el virus sino un tratamiento para enfermos graves a los que ayudan a mejorar su recuperación y sus condiciones hospitalarias. Gilead comercializará este medicamento con el nombre de Veklury, y ya se estaba utilizando en pacientes con la enfermedad, de modo experimental, de hecho el propio presidente Trump, la recibió cuando se contagió con el virus.
La medida se produce a pesar de que la Organización Mundial de la Salud, publicaba los resultados de un estudio completo la pasada semana, en la que quedaba claro que el remdesivir no ayudó a reducir las muertes de pacientes hospitalizados por COVID-19. Algunos científicos y médicos señalaron que el estudio de la OMS no podía ser concluyente por la metodología utilizada, aunque en los datos recabados disponibles en la página del Organización Mundial de la Salud, recaban datos de cientos de hospitales en 30 países.
Con estos permisos, el remdesivir se convierte en el único tratamiento autorizado en EEUU para el coronavirus, que ha infectado a mas de 41 millones de personas en todo el mundo, aunque existen otros tratamientos que tienen autorización de uso de emergencia, como es el caso del plasma.
La farmacéutica espera fabricar solo este año más de 2.000.000 de dosis del medicamento, que se administra por vía intravenosa.
Los críticos dicen que el propósito de la autorización de la Agencia de Medicamentos es contrarrestar el jarro de agua fría que supuso el informe de la OMS en el que presentaba, con datos empíricos, la ineficacia de los tratamientos antivirales usados hasta ahora y que incluyen la hidroxicloroquina, el remdesivir, el lopinavir y el interferon .

Victoria García
En la SER, desde hace casi tres décadas, con algunas ausencias. Antes en Antena3 Radio y TV. Trabajé...





