Denuncian que no hay coordinación entre los ensayos clínicos sobre coronavirus
La organización Salud por Derecho asegura, después de analizar los ensayos publicados en el del Registro Español de Ensayos Clínicos (REec) desde el inicio de la pandemia, que el 90% analiza fármacos que se repiten en diferentes estudios sin conexión entre ellos

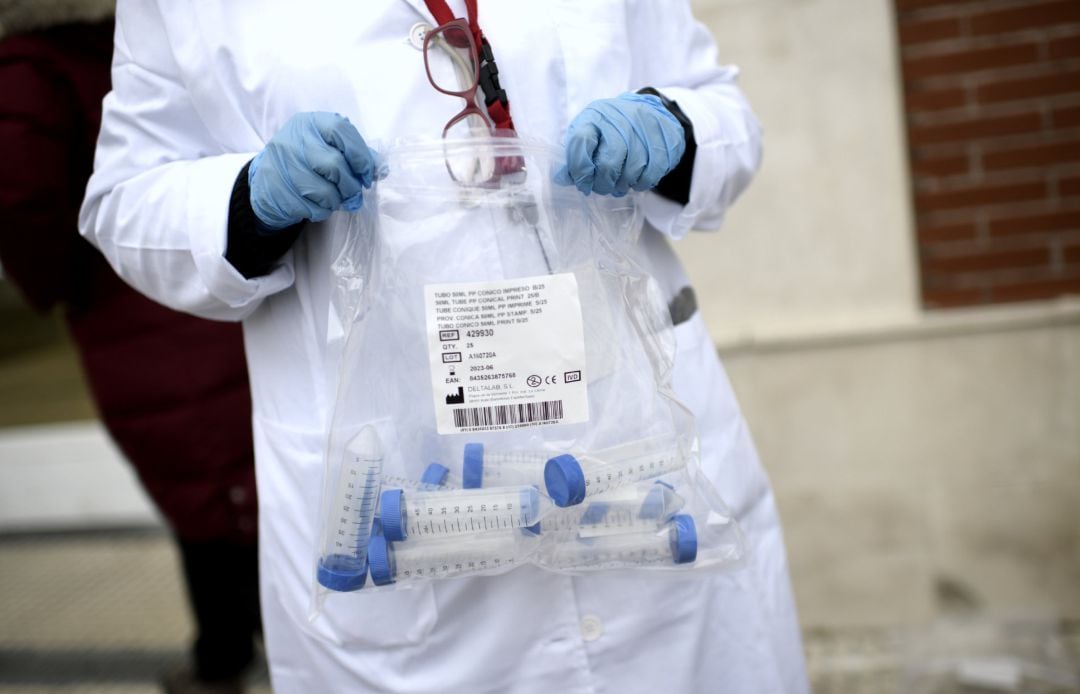
Un sanitario con tubos de ensayo durante la realización de tests. / Óscar Cañas - Europa Press (EUROPA PRESS)
Madrid
A 1 de octubre de 2020, en España, había 123 ensayos relacionados con la COVID-19 que evalúan 76 productos diferentes. De ellos, el 91% (113 ensayos) analizan fármacos, ya sea para la COVID-19 o para sus complicaciones. Para Eva Iraizoz, investigadora de Salud por Derecho y coautora del informe: "Llama la atención la escasa diversidad de medicamentos evaluados y el número elevado de ensayos sobre los mismos medicamentos, como en el caso de la hidroxicloroquina, presente en 20 ensayos diferentes."
Estos datos apuntan, según Salud Por Derecho, a que las iniciativas de investigación clínica españolas sobre la COVID-19 pueden estar fragmentadas y duplicadas. "La proliferación de ensayos clínicos pequeños sobre un mismo medicamento no parece la manera más eficaz de generar el conocimiento y de contribuir a un avance rápido en la lucha contra la COVID-19. Más bien corremos el riesgo de que esta atomización que estamos viendo conlleve un malgasto de recursos de investigación".
Casi la mitad no publica resultados
En el estudio que esta organización ha realizado en colaboración con Universities Allied for Essential Medicines (UAEM Europa) y TranspariMED, también han analizado la transparencia de los ensayos clínicos españoles en el Registro Europeo y la conclusión no es positiva: casi la mitad (44%) de los principales responsables de los ensayos clínicos de nuestro país no publican los resultados de sus ensayos.
Según la normativa vigente los responsables de los ensayos están obligados a enviar al Registro Europeo de Ensayos Clínicos (EudraCT) un informe de resultados 12 meses después de haber concluido la investigación, pero parece que es habitual lo de incumplir los plazos. "En nuestro país, dice Iraizoz, "las 32 principales entidades españolas responsables de ensayos clínicos suman un total de 1036 ensayos. De ellos, 142 aparecen como finalizados hace más de un año y, por tanto, deberían tener los resultados publicados. Sin embargo, solo el 56% (80) lo ha hecho. Es decir, un 44% de los ensayos que deberían haber publicado sus resultados no lo hicieron."
Solo tres cumplen fielmente
De las 32 entidades responsables analizadas, únicamente tres han cumplido fielmente con las exigencias de las normas de transparencia europeas. Otras cinco han divulgado solo algunos de sus resultados y el resto no ha publicado nada.
Con estos datos, Salud por derecho pide a las entidades financiadoras, en el caso de España el Instituto de Salud Carlos III que "tengan un mayor control de los ensayos y que la transparencia sea una condición a la financiación". A la Agencia Española de Medicamentos y Productos Sanitarios le exigen que haga un seguimiento de los registros y que se impongan sanciones a los promotores que incumplan de forma reiterada con la transparencia.





