AstraZeneca reconoce que los datos de su ensayo en EEUU estaban desactualizados y aportará nuevos en 48 horas
EEUU alertaba de que los datos proporcionados por la farmacéutica desactualizados y la compañía ha reconocido que, efectivamente, eran anteriores al 17 de febrero pero que "inmediatamente" aportará los nuevos

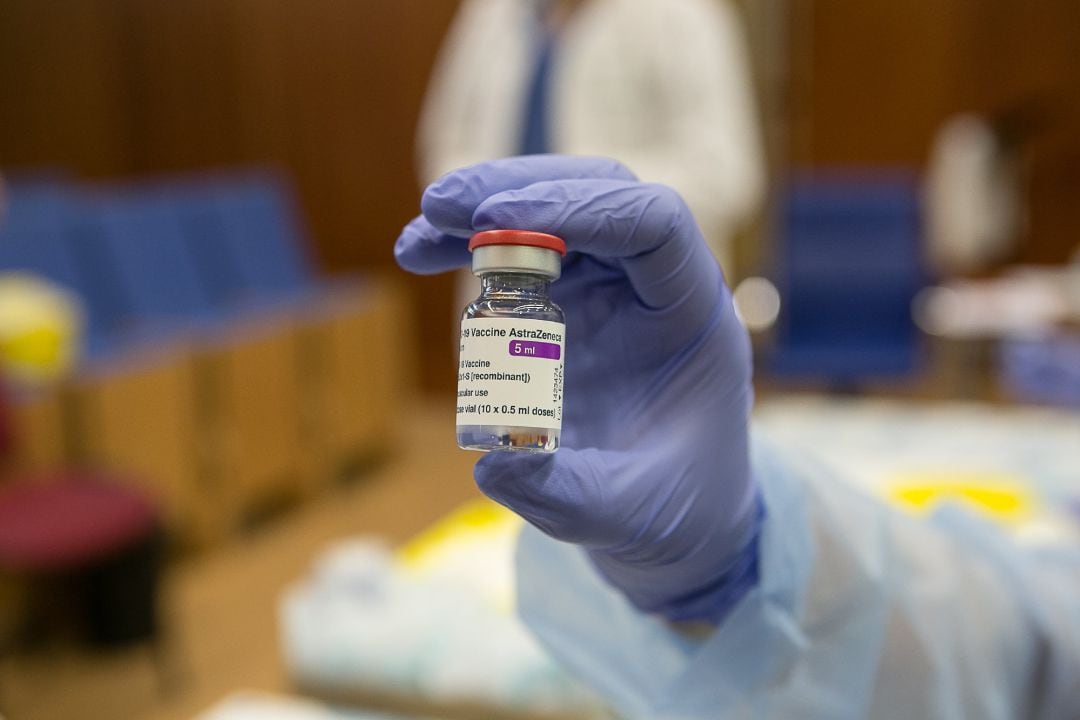
Una profesional sanitaria sostiene un vial de la vacuna AstraZeneca contra la COVID-19 / Jorge Armestar (EUROPA PRESS)
Londres
La farmacéutica anglo-sueca AstraZeneca ha indicado este martes que difundirá en 48 horas los datos del "análisis primario" de su ensayo clínico sobre la vacuna contra la COVID-19 en Estados Unidos, tras reconocer que las cifras divulgadas este lunes eran anteriores al 17 de febrero.
En un comunicado, la compañía admitía que los resultados dados a conocer eran un "análisis provisional" con datos de hasta el 17 de febrero, pero que "inmediatamente" contactarán con el Consejo de Monitoreo de Datos y Seguridad de EEUU (DSMB, por sus siglas en inglés), integrado por un panel de expertos independiente que asesora al Gobierno, para darle cifras actualizadas.
El DSMB expresó este lunes su preocupación por la información publicada por AstraZeneca, al considerar que podía usar datos obsoletos. En los resultados difundidos la empresa decía que el preparado tiene una efectividad del 79 % en la prevención de síntomas de la COVID. "Contactaremos inmediatamente con el DSMB para compartir nuestro análisis primario con los datos sobre eficacia más actualizados. Pretendemos sacar los resultados del análisis primario en 48 horas", subraya la nota. Y agrega que la evaluación que han hecho del mencionado "análisis primario" muestra que sus resultados son "consistentes" con los provisionales difundidos este lunes.
El DSMB informó a última hora de este lunes al Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos (NIAID, en sus siglas en inglés) de su preocupación por la posible información desactualizada, "que puede haber proporcionado una visión incompleta de los datos de eficacia".
Descubre la nueva app de Cadena SER Te ofrecemos una mejor experiencia de audio y video
Descargar"Instamos a la empresa (AstraZeneca) a trabajar con el DSMB para revisar los datos de eficacia y garantizar que estas cifras de eficacia más precisas y actualizadas se hagan públicas lo antes posible", subrayó el NIAID.
Antes de conocer esa opinión de sus científicos, la Casa Blanca describió como "alentador" el estudio sobre los ensayos clínicos de la vacuna de AstraZeneca, que indicaban que ese producto muestra un 79% de efectividad previniendo la COVID-19 sintomática y ofrece protección del 100% ante la enfermedad grave y la hospitalización.





